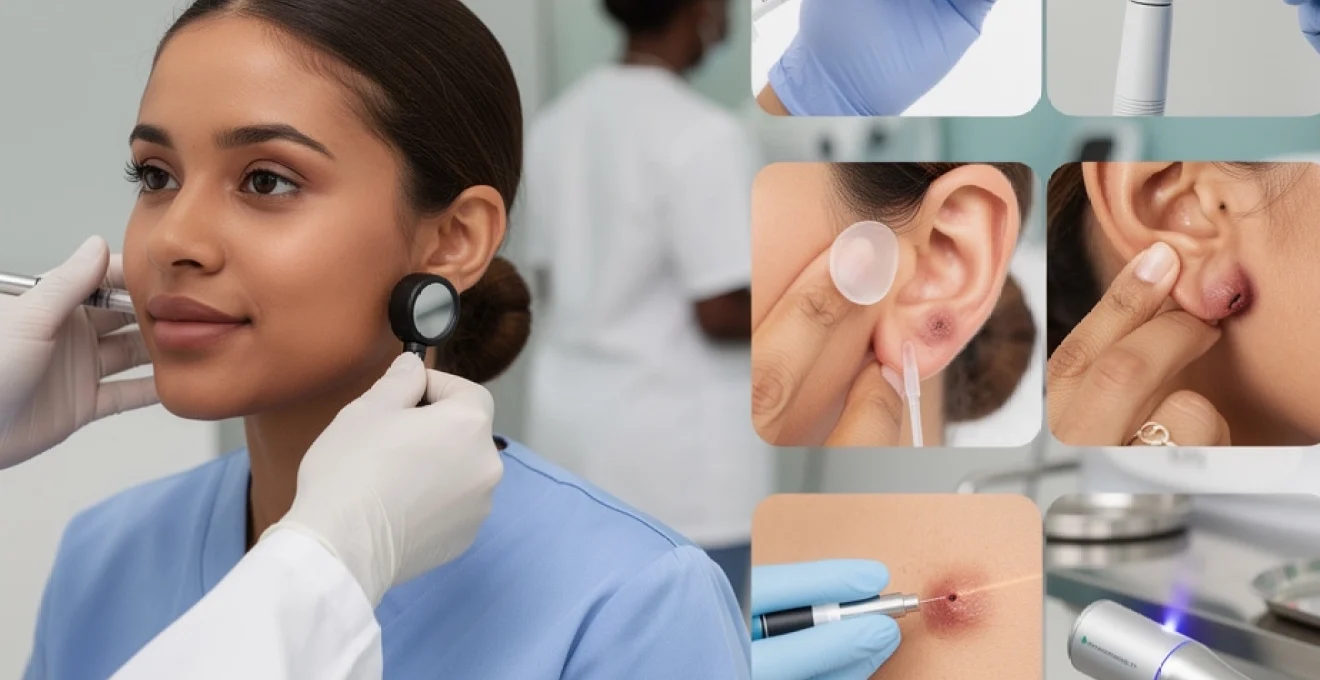
Les chéloïdes représentent une complication redoutée dans l’univers du piercing, touchant environ 15% des personnes ayant réalisé une perforation cutanée. Ces cicatrices pathologiques, caractérisées par une prolifération excessive de tissu conjonctif, peuvent transformer une simple modification corporelle en véritable défi thérapeutique. Contrairement aux idées reçues, toutes les excroissances post-piercing ne constituent pas des chéloïdes véritables, d’où l’importance cruciale d’un diagnostic différentiel précis.
La prise en charge thérapeutique des chéloïdes post-piercing a considérablement évolué ces dernières années, intégrant des approches multimodales combinant traitements topiques, injections intra-lésionnelles et techniques chirurgicales avancées. L’efficacité thérapeutique dépend largement de la précocité du diagnostic et de l’adaptation du protocole de soins aux caractéristiques individuelles du patient.
Identification et diagnostic différentiel des chéloïdes post-piercing
Caractéristiques histopathologiques des chéloïdes versus cicatrices hypertrophiques
L’analyse histopathologique révèle des différences fondamentales entre chéloïdes et cicatrices hypertrophiques. Les chéloïdes présentent une désorganisation caractéristique des fibres de collagène, formant des nodules épais et des faisceaux entrecroisés. La composition en collagène type III s’avère significativement augmentée par rapport au collagène type I, créant une matrice extracellulaire pathologique. Cette architecture désorganisée explique la texture ferme et l’aspect brillant typiques des chéloïdes.
Les cicatrices hypertrophiques, contrairement aux chéloïdes, maintiennent une organisation parallèle des fibres de collagène et respectent généralement les limites de la blessure initiale. Cette distinction histologique s’accompagne de différences cliniques majeures : les cicatrices hypertrophiques tendent vers la régression spontanée, tandis que les chéloïdes persistent et peuvent s’étendre au-delà du site de piercing initial.
Localisation anatomique à risque : cartilage auriculaire et septum nasal
Certaines localisations anatomiques présentent une susceptibilité accrue au développement chéloïdien. Le cartilage auriculaire, particulièrement l’hélix et le tragus, concentre près de 60% des cas de chéloïdes post-piercing. Cette prédisposition s’explique par la faible vascularisation cartilagineuse et la tension mécanique constante exercée sur ces zones. Le septum nasal constitue également un site à risque élevé, avec une incidence chéloïdienne de 25% selon les études récentes.
La région du décolleté et les lobes d’oreilles complètent le tableau des localisations préférentielles. L’épaisseur dermique variable et la mobilité tissulaire de ces régions favorisent les phénomènes inflammatoires chroniques, précurseurs du développement chéloïdien. L’identification précoce de ces facteurs de risque anatomiques permet d’adapter les protocoles préventifs et thérapeutiques.
Facteurs prédisposants génétiques et phénotype fitzpatrick IV-VI
La prédisposition génétique joue un rôle déterminant dans la genèse chéloïdienne. Les individus présentant un phototype Fitzpatrick IV à VI affichent une incidence chéloïdienne 10 à 15 fois supérieure aux
à celle observée chez les phototypes I à III. Cette susceptibilité accrue serait liée à des variations génétiques affectant la régulation de la synthèse du collagène, notamment au niveau des voies TGF-β et des facteurs de croissance fibroblastiques. Des antécédents familiaux de chéloïdes, de cicatrices hypertrophiques ou de « boules de chair » après traumatismes cutanés banals doivent alerter avant tout projet de piercing.
Chez ces patients à risque, la prise de décision doit être particulièrement prudente : information claire sur la probabilité de chéloïde, choix de zones moins à risque (éviter le cartilage auriculaire, par exemple) et protocole de surveillance rapprochée. En pratique, si vous savez que vous ou un proche avez déjà présenté des chéloïdes après une chirurgie, un vaccin ou un simple perçage de l’oreille, il est pertinent de discuter avec un dermatologue avant de réaliser un nouveau piercing.
Critères cliniques de la classification de vancouver pour cicatrices pathologiques
La classification de Vancouver (Vancouver Scar Scale, VSS) constitue un outil de référence pour évaluer la sévérité des cicatrices pathologiques, incluant les chéloïdes post-piercing. Elle repose sur quatre items cliniques : la vascularisation (couleur), l’épaisseur, la souplesse (ou « pliabilité ») et la pigmentation. Chaque critère est coté, permettant d’obtenir un score global, plus il est élevé, plus la cicatrice est considérée comme sévère.
Concrètement, une chéloïde de piercing se caractérise souvent par une coloration rouge à violacée (hypervascularisation), une épaisseur nettement augmentée par rapport à la peau adjacente, une consistance ferme voire caoutchouteuse, et une hyperpigmentation chez les phototypes foncés. L’utilisation de la classification de Vancouver permet non seulement d’objectiver l’évolution sous traitement, mais aussi de comparer l’efficacité des différentes stratégies thérapeutiques au fil du suivi.
Protocoles thérapeutiques topiques et injection intra-lésionnelle
Corticothérapie intra-lésionnelle : triamcinolone acétonide 10-40 mg/ml
La corticothérapie intra-lésionnelle par triamcinolone acétonide demeure le gold standard dans le traitement des chéloïdes post-piercing. Le principe ? Injecter directement dans la masse chéloïdienne un corticoïde retard à forte concentration (généralement entre 10 et 40 mg/ml), afin d’inhiber la prolifération fibroblastique et la synthèse de collagène. Cette approche vise à aplatir progressivement la lésion, réduire les démangeaisons et atténuer la douleur.
En pratique, les injections sont réalisées toutes les 4 à 6 semaines, sur une durée moyenne de 3 à 6 séances selon le volume et l’ancienneté de la chéloïde. Plus la chéloïde est récente, plus la réponse au traitement est favorable. Le dermatologue ajuste la concentration (10, 20 ou 40 mg/ml) en fonction de l’épaisseur de la lésion et de la tolérance cutanée. Pour vous, cela signifie que la régularité des séances est essentielle : interrompre trop tôt le protocole augmente le risque de récidive partielle.
Comme tout traitement puissant, les injections de triamcinolone ne sont pas exemptes d’effets secondaires : atrophie cutanée localisée, télangiectasies, hypopigmentation en halo autour de la lésion. Ces effets sont généralement limités lorsque le protocole est bien mené (volume injecté modéré, espacement suffisant des séances). Un dialogue franc avec votre médecin permet d’ajuster la fréquence et la dose pour optimiser le rapport bénéfice–risque.
Application de gel de silicone médical et pansements compressifs mepiform
Les gels siliconés et les pansements en silicone type Mepiform représentent une pierre angulaire du traitement topique des chéloïdes de piercing, en particulier pour les lésions de petite à moyenne taille sur le lobe de l’oreille. Le silicone crée un micro-environnement occlusif et hydraté qui modifie la tension superficielle de la peau, régule la production de collagène et améliore la souplesse de la cicatrice. Utilisés de façon précoce, ces dispositifs permettent souvent de limiter la progression de la lésion.
Le protocole classique consiste à appliquer une fine couche de gel de silicone médical deux fois par jour, sur peau propre et sèche, ou à porter un pansement siliconé mince (type Mepiform) 12 à 24 heures par jour pendant plusieurs mois. L’analogie la plus parlante est celle d’un « film protecteur intelligent » qui apprend à la peau à cicatriser de manière plus ordonnée. Chez les porteurs de piercing, ces pansements peuvent être découpés sur mesure pour épouser la forme du lobe en laissant passer la tige du bijou.
Associés à une thérapie compressive légère (par exemple, boucles de pression ou pastilles siliconées avant/arrière autour du bijou), ces dispositifs augmentent l’efficacité globale du traitement. Vous pouvez les envisager comme un complément essentiel aux injections : les corticoïdes modulent la réponse inflammatoire en profondeur, le silicone stabilise ensuite la surface et participe à la prévention des récidives.
Thérapie par injection de 5-fluorouracile combinée aux corticoïdes
Pour les chéloïdes résistantes à la corticothérapie seule, la combinaison triamcinolone acétonide–5-fluorouracile (5-FU) présente des résultats très encourageants. Le 5-FU est un antimitotique qui bloque la prolifération des fibroblastes et des myofibroblastes responsables de l’excès de collagène. Injecté en mélange avec la triamcinolone dans la lésion, il potentialise l’effet anti-fibrosant tout en permettant d’utiliser des doses de corticoïdes plus faibles.
Les protocoles les plus utilisés associent par exemple 0,1 à 0,2 ml de triamcinolone (10–20 mg/ml) à 0,8–0,9 ml de 5-FU (50 mg/ml) par séance, administrés toutes les 3 à 4 semaines. Cliniquement, on observe souvent un ramollissement rapide de la chéloïde, suivi d’un aplatissement progressif et d’une diminution des symptômes (prurit, douleurs). Il s’agit d’une option particulièrement intéressante pour les chéloïdes volumineuses des lobes d’oreilles liées aux piercings pesants ou aux élargissements progressifs.
Le revers de la médaille ? Les injections de 5-FU peuvent être plus douloureuses localement, et entraîner des réactions inflammatoires transitoires (érythème, œdème). Un anesthésique local ou l’application préalable d’une crème anesthésiante peut améliorer considérablement le confort des séances. Si vous appréhendez la douleur, n’hésitez pas à en parler à votre dermatologue pour adapter le protocole.
Cryothérapie à l’azote liquide : protocole freeze-thaw cyclique
La cryothérapie à l’azote liquide repose sur un principe simple : exposer la chéloïde à un froid extrême (–196 °C) par cycles de congélation–décongélation, afin de détruire sélectivement le tissu fibro-cicatriciel. Ce protocole « freeze-thaw cyclique » provoque une nécrose contrôlée de la lésion, suivie d’une réorganisation plus harmonieuse du collagène lors de la réparation. Les chéloïdes de petite taille (notamment sur lobes d’oreille) répondent particulièrement bien à cette approche.
En pratique, le dermatologue applique une sonde ou un spray d’azote liquide pendant 10 à 30 secondes, laisse la lésion décongeler, puis répète le cycle une à trois fois au cours de la même séance. Les sessions sont espacées de 4 à 6 semaines, avec généralement 2 à 4 séances nécessaires. L’association de la cryothérapie avec des injections de triamcinolone ou de 5-FU permet d’optimiser les résultats, en particulier pour les chéloïdes épaisses post-piercing qui résistent aux monothérapies.
La principale limite de la cryothérapie est le risque de dyschromies (taches plus claires) chez les phototypes foncés, ainsi que la formation de phlyctènes et de croûtes transitoires. Vous devrez donc prévoir quelques jours pendant lesquels la zone traitée sera plus visible, avant d’évoluer vers une cicatrice plus plate. Là encore, le choix du protocole se fait au cas par cas, en concertation étroite avec votre médecin.
Techniques chirurgicales et thérapies physiques avancées
Excision chirurgicale avec radiothérapie adjuvante post-opératoire
Lorsque la chéloïde de piercing est volumineuse, très symptomatique ou invalidante sur le plan esthétique, l’excision chirurgicale peut être envisagée. Cependant, retirer la chéloïde seule n’est jamais suffisant : le taux de récidive après chirurgie isolée peut atteindre 80 à 100 %. C’est pourquoi cette option doit systématiquement s’intégrer dans une stratégie combinée, dont la radiothérapie adjuvante post-opératoire est un pilier majeur.
Le principe est d’exciser la chéloïde en respectant au maximum les plans anatomiques, puis d’appliquer dans les 24 à 72 heures un traitement par radiothérapie à faible dose sur la zone opérée. Ces doses ciblées (généralement 12 à 20 Gy fractionnés) inhibent la reprise de prolifération des fibroblastes responsables de la récidive. Des études récentes montrent que cette approche combinée réduit le taux de récidive à moins de 20–30 % pour les chéloïdes d’oreille post-piercing.
Ce type de prise en charge nécessite un plateau technique spécialisé et une coordination étroite entre chirurgien, radiothérapeute et dermatologue. Pour le patient, cela implique plusieurs rendez-vous rapprochés mais, en contrepartie, une amélioration esthétique souvent spectaculaire. Il s’agit d’une option de référence pour les chéloïdes « rebelles » ayant déjà récidivé après traitements conservateurs.
Laser CO2 fractionné et laser à colorant pulsé 595 nm
Les lasers occupent une place croissante dans le traitement avancé des chéloïdes de piercing, en complément des corticoïdes et du silicone. Le laser CO2 fractionné agit comme un « sculptant » micro-ablatif : il crée des micro-colonnes de vaporisation dans la lésion, stimulant un remodelage profond du collagène. Résultat : une cicatrice plus plane, plus souple et une meilleure intégration esthétique dans la peau environnante.
Le laser à colorant pulsé (PDL) à 585–595 nm cible quant à lui sélectivement l’hémoglobine, réduisant la vascularisation excessive des chéloïdes récentes. Il permet d’atténuer les rougeurs, de diminuer le prurit et, utilisé précocement, de limiter l’épaississement secondaire. Dans le contexte d’une chéloïde de piercing, l’association CO2 fractionné + PDL, parfois complétée par des injections intra-lésionnelles, constitue un véritable « kit de remodelage » sur-mesure.
Le choix du type de laser, des paramètres (énergie, densité, nombre de passages) et de la fréquence des séances dépend de nombreux facteurs : taille, ancienneté de la chéloïde, phototype cutané, tolérance aux suites (érythème, croûtes temporaires). Si vous envisagez cette option, il est essentiel de consulter un dermatologue ou un médecin esthétique expérimenté en laser, car une mauvaise indication ou des réglages inadaptés peuvent au contraire majorer le risque de dyschromies.
Thérapie par pression dynamique et compression élastique graduée
La thérapie compressive est une stratégie simple en apparence, mais redoutablement efficace sur les chéloïdes de lobe d’oreille. Le principe est d’appliquer une pression mécanique continue et contrôlée sur la cicatrice, par l’intermédiaire de dispositifs adaptés : boucles d’oreille de pression, clips compressifs sur mesure, pastilles siliconées ou orthèses spécifiques. Cette pression constante diminue l’apport sanguin local, réduit l’activité des fibroblastes et favorise l’aplatissement progressif de la lésion.
Dans le cas des chéloïdes post-piercing, l’objectif est de maintenir une pression de 20 à 30 mmHg environ, pendant plusieurs heures par jour, sur une durée minimale de 3 à 6 mois. Cela peut paraître contraignant, mais les résultats sont souvent à la hauteur des efforts : diminution nette du volume, meilleure texture, réduction des symptômes. Cette approche est fréquemment combinée à des corticoïdes intra-lésionnels ou au silicone pour une efficacité maximale.
Pour bien comprendre, imaginez la cicatrice comme une mousse qui gonfle lorsque rien ne la contient : la compression agit comme une main douce mais ferme, qui limite ce gonflement et guide la peau vers une forme plus harmonieuse. Une bonne observance (port quotidien, respect des consignes d’hygiène, contrôle régulier chez le spécialiste) est la clé du succès de cette technique.
Microneedling associé aux facteurs de croissance plaquettaires
Le microneedling, ou thérapie par micro-aiguilles, consiste à créer de multiples micro-perforations contrôlées dans la surface de la chéloïde à l’aide de dispositifs spéciaux (dermaroller, stylo électrique). Ces micro-canaux induisent un remodelage du collagène et permettent la pénétration de substances actives. Quand il est associé au plasma riche en plaquettes (PRP), riche en facteurs de croissance, il ouvre des perspectives intéressantes dans la gestion des cicatrices difficiles.
Dans le contexte des chéloïdes post-piercing, le microneedling-PRP est généralement envisagé en phase de stabilisation ou en complément d’autres traitements (corticoïdes, silicone, laser). Le PRP, préparé à partir du propre sang du patient, est appliqué ou injecté localement après le microneedling, favorisant une cicatrisation plus équilibrée et moins fibreuse. Pensez-y comme à un « reset » partiel de la cicatrice, où l’on propose à la peau de réécrire une version plus douce de son histoire.
Cette approche reste toutefois réservée à des équipes expérimentées et nécessite une bonne sélection des indications. Elle ne remplace pas les traitements de référence, mais peut les compléter efficacement, notamment chez les patients motivés souhaitant optimiser le résultat esthétique final après la phase aiguë de traitement.
Prévention et surveillance post-thérapeutique des récidives
La prévention des chéloïdes post-piercing commence avant même la réalisation du trou. Chez un patient à risque (phototype foncé, antécédents de chéloïdes, localisation cartilagineuse), il est souvent plus prudent de renoncer à certains piercings à haut risque ou de privilégier des zones cutanées moins sujettes à la sur-cicatrisation. Le choix du perceur, de la technique (aiguille stérile plutôt que pistolet) et du bijou (titane ASTM F-136, or 14/18 carats sans nickel) joue un rôle central dans la réduction du traumatisme initial.
Après le piercing, une hygiène rigoureuse mais non agressive est de mise : nettoyage biquotidien au sérum physiologique, séchage par tamponnement avec compresse stérile, éviction des antiseptiques forts en l’absence de réelle infection. Il convient également de limiter au maximum les traumatismes mécaniques : éviter de dormir sur le piercing, proscrire les frottements répétés (casques, écouteurs, vêtements serrés), ne pas manipuler ni tourner le bijou sans nécessité. Ce sont souvent ces « petits détails du quotidien » qui font toute la différence dans la prévention d’une excroissance.
Après traitement d’une chéloïde avérée, la surveillance post-thérapeutique est cruciale car la récidive peut survenir dans les mois qui suivent. Des consultations de contrôle régulières (tous les 3 à 6 mois la première année) permettent de détecter précocement tout signe de reprise évolutive : épaississement localisé, rougeur persistante, démangeaisons. À ce stade, une simple reprise des traitements topiques ou quelques séances supplémentaires d’injections peuvent suffire à contrôler la situation, évitant ainsi une nouvelle évolution majeure.
Complications et contre-indications thérapeutiques spécifiques
Chaque modalité thérapeutique des chéloïdes post-piercing comporte des bénéfices, mais aussi des risques potentiels qu’il est indispensable de connaître. Les corticoïdes intra-lésionnels, par exemple, peuvent entraîner une atrophie cutanée, des télangiectasies ou une hypopigmentation, en particulier chez les phototypes foncés. La cryothérapie peut majorer ces troubles pigmentaires et provoquer des cicatrices atrophiques si elle est trop agressive. Quant aux lasers, ils requièrent un réglage très précis pour éviter brûlures et dyschromies persistantes.
La radiothérapie adjuvante, bien que très efficace pour limiter les récidives après excision, doit être utilisée avec discernement, notamment chez les sujets jeunes, en raison des interrogations théoriques sur le risque carcinologique à long terme. De même, les injections de 5-FU sont contre-indiquées chez la femme enceinte et chez certains patients présentant des troubles hématologiques ou une intolérance documentée. Votre médecin passera systématiquement en revue vos antécédents et traitements en cours avant de valider un protocole.
Enfin, il est important de distinguer les complications des chéloïdes elles-mêmes (douleur chronique, gêne fonctionnelle si lésion volumineuse, impact psychologique majeur) des effets secondaires des traitements. La bonne nouvelle, c’est qu’en adoptant une approche individualisée, prudente et progressive, la majorité de ces risques peuvent être anticipés et minimisés. N’hésitez pas à poser toutes vos questions : plus vous comprenez les enjeux de chaque option, plus vous pouvez prendre une décision éclairée concernant votre piercing et son traitement.
Approches thérapeutiques émergentes et médecine régénérative
La prise en charge des chéloïdes de piercing bénéficie aujourd’hui de l’essor de la médecine régénérative et des thérapies ciblées. Des molécules modulant spécifiquement les voies de signalisation impliquées dans la fibrose, comme les inhibiteurs de TGF-β, de PDGF ou certaines cytokines pro-fibrotiques, sont en cours d’évaluation. L’objectif est d’agir « en amont » de la cascade cicatricielle, pour empêcher la formation même du tissu chéloïdien plutôt que de le corriger a posteriori.
Parallèlement, des biothérapies innovantes, telles que l’utilisation de cellules souches mésenchymateuses ou de matrices extracellulaires biosynthétiques, commencent à être explorées. L’idée est de fournir à la peau un environnement de réparation plus physiologique, capable de guider les fibroblastes vers une cicatrisation normale. Si ces approches restent encore largement du domaine de la recherche, elles laissent entrevoir, à moyen terme, des solutions plus durables et moins invasives pour les personnes sujettes aux chéloïdes récurrentes.
Pour vous, en tant que porteur ou futur porteur de piercing, cela signifie qu’il devient de plus en plus possible de personnaliser les traitements en fonction de votre profil de risque, de votre phototype et de vos attentes esthétiques. En combinant les stratégies éprouvées (corticoïdes, silicone, compression, laser) avec ces nouvelles pistes, la gestion des chéloïdes post-piercing s’oriente vers une approche véritablement sur-mesure, où l’on ne se contente plus de « faire disparaître une boule », mais où l’on accompagne votre peau vers une cicatrisation la plus harmonieuse possible.